Тема 34. Растворы. Растворение. - cтраницы 161, 162, 163, 164, 165, 166
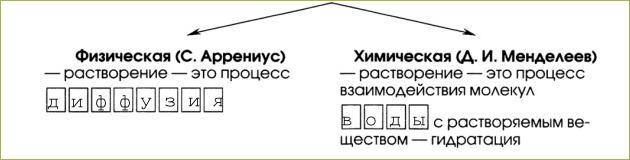
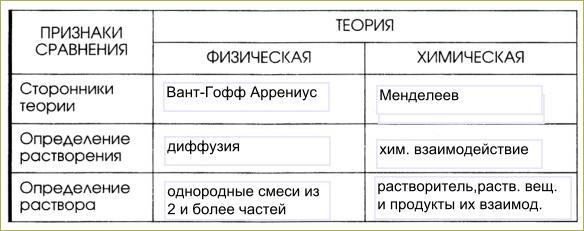
1. Растворы - это гомогенные смеси, состоящие из 2 или более однородных частей, то есть частиц растворённого вещества, растворителя и продуктов их взаимодействия.
3. Гидратация - это взаимодействие молекул вещества с водой.
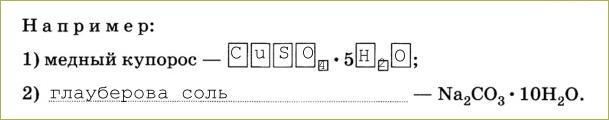
Кристаллогидраты - это соли, в состав которых входит вода.
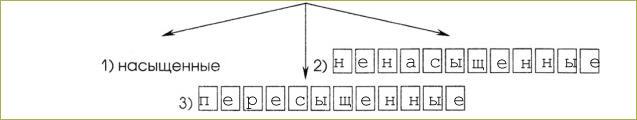
4. Различают растворы
Дайте определение каждого типа растворов.- раствор, в котором при данной температуре вещество больше не растворяется.
- раствор, в котором при данной температуре меньше раств. вещества, чем в насыщенном.
- раствор, в котором больше вещества, чем в насыщенном.
- При добавлении соли в воду происходит процесс химического взаимодействия.
- В растворе одновременно находятся и растворённое вещество, и растворитель, и продукты их взаимодействия.
- Растворение также процесс, в результате которого имеют место и тепловые явления.
5. Заполните текст формулами и названиями соединений, числовыми значениями.
Примечание. Воспользуйтесь данными графиков растворимости веществ (см. рис. 126 в учебнике) и таблицей растворимости.
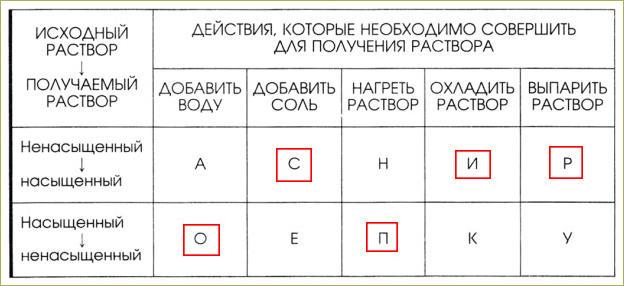
6. Установите соответствие между действием, которое нужно совершить для получения раствора, и типом раствора. Из букв, соответствующих правильным ответам, вы составите название раствора сахара в воде: сироп.
7. Растворимость хлорида калия в воде при 60 °С равна 50 г. Определите массовую долю соли в растворе, насыщенном при указанной температуре.
8. По графику (см. рис. 126 в учебнике) определите растворимость сульфата калия при 80 °С. Рассчитайте массовую долю соли в растворе, насыщенном при указанной температуре.
9. Навеску 161 г глауберовой соли Na2S04 • ЮН20 растворили в 180 л воды. Вычислите массовую долю сульфата натрия в полученном растворе. Сколько ионов каждого вида в нём находится?
Сохраните или поделитесь с одноклассниками: