Щелочные металлы - cтраницы 151, 152, 153, 154, 155, 156
1. Начертите схему строения атома рубидия Rb. Сравните ее со схемами строения атомов натрия и цезия.
2. Почему все щелочные металлы – сильные восстановители?
Щелочные металлы легко отдают свой валентный электрон, являясь сильными восстановителями.
3. Сравните реакции щелочных металлов с водой и с кислотами. Составьте уравнения соответствующих реакций и покажите переход электронов.
4. Сколько граммов раствора, содержащего 0,1 массовой доли, или 10%, гидроксида натрия, потребуется для нейтрализации 196 г раствора, содержащего 0,1 массовой доли, или 10%, серной кислоты?
5. При обработке 15 г технической поваренной соли концентрированной серной кислоты выделилось 5,6 л газа (н.у.). Рассчитайте массовую долю (в процентах) примесей в поваренной соли.
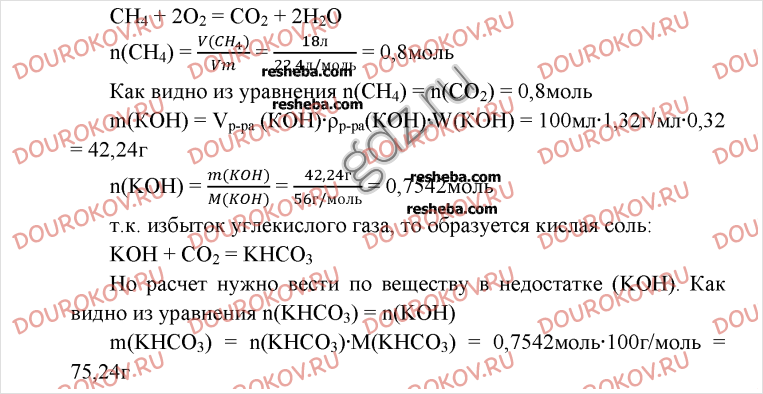
6. Определите, какая соль получится, и рассчитайте ее массу, если через 100 мл раствора, содержащего 0,32 массовой доли, или 32%, гидроксида калия (p=1,32г/см3), пропустили весь оксид углерода (IV), который образуется при сжигании 18 л метана (н.у.).
ТЕСТОВЫЕ ЗАДАНИЯ
1. Химический элемент, атомная масса которого 23, а число нейтронов в ядре равно 12, в периодической системе находится
4) в 3-м периоде, IА-группе
2. При взаимодействии калия с водой наряду с водородом образуется
2) гидроксид
3. Необходимо строго соблюдать правила безопасности, работая с веществом
2) KOH
Сохраните или поделитесь с одноклассниками: