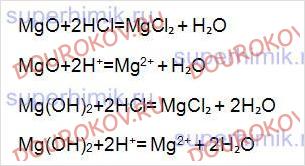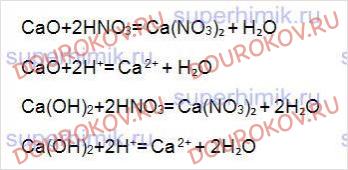Характеристика элемента по его положению в Периодической системе химических элементов Д. И. Менделеева. Химические реакции. 1 уровень - cтраницы 104, 105, 106, 107
ВАРИАНТ 1
ЗАДАНИЕ 1
Дано уравнение реакции нейтрализации гидроксида натрия соляной кислотой: NaOH + НСl = NaCl + Н20 + Q.
Дайте характеристику реакции по следующим признакам:
- число и состав исходных веществ и продуктов реакции;
- тепловой эффект;
- агрегатное состояние веществ;
- участие катализатора;
- изменение степеней окисления элементов;
- направление.
ЗАДАНИЕ 2
Дайте характеристику химического элемента магния по плану:
- положение элемента в ПСХЭ;
- строение атома;
- формулы оксида и гидроксида, их характер.
ЗАДАНИЕ 3
Напишите уравнения реакций оксида и гидроксида магния с соляной кислотой в молекулярном и ионном виде.
ВАРИАНТ 2
ЗАДАНИЕ 1Дана схема реакции горения алюминия Аl + 02 → А1203 + Q.
Составьте уравнение данной реакции, расставив коэффициенты в нем методом электронного баланса. Укажите окислитель и восстановитель.
Дайте характеристику реакции по следующим признакам:
- число и состав исходных веществ и продуктов реакции;
- тепловой эффект;
- агрегатное состояние веществ;
- участие катализатора;
- изменение степеней окисления элементов;
- направление.
Дайте характеристику химического элемента натрия по плану:
- положение элемента в ПСХЭ;
- строение атома;
- формулы оксида и гидроксида, их характер.
ЗАДАНИЕ 3
Напишите уравнения реакций оксида и гидроксида натрия с раствором серной кислоты в молекулярном и ионном виде.
ВАРИАНТ 3
ЗАДАНИЕ 1Дана схема реакции получения оксида серы (VI) из оксида серы (IV) S02 + 02 -> S03 + Q.
Составьте уравнение данной реакции, расставив коэффициенты в нем методом электронного баланса. Укажите окислитель и восстановитель.
Дайте характеристику реакции по следующим признакам:
- число и состав исходных веществ и продуктов реакции;
- тепловой эффект;
- агрегатное состояние веществ;
- участие катализатора;
- изменение степеней окисления элементов;
- направление.
ЗАДАНИЕ 2
Дайте характеристику химического элемента лития по плану:
- положение элемента в Периодической системе;
- строение атома;
- формулы оксида и гидроксида, их характер.
ЗАДАНИЕ 3
Напишите уравнения реакций оксида и гидроксида лития с серной кислотой в молекулярном и ионном виде.
ВАРИАНТ 4
ЗАДАНИЕ 1
Дано уравнение реакции цинка с соляной кислотой: Zn + 2НСl = ZnCl2 + Н2↑ + Q.Дайте характеристику реакции по следующим признакам:
- число и состав исходных веществ и продуктов реакции;
- тепловой эффект;
- агрегатное состояние участвующих в реакции веществ;
- участие катализатора;
- изменение степеней окисления химических элементов;
- направление.
ЗАДАНИЕ 2
Дайте характеристику химического элемента кальция по плану:
- положение элемента в Периодической системе;
- строение атома;
- формулы высшего оксида и гидроксида, их характер.
ЗАДАНИЕ 3
Напишите уравнения реакций оксида и гидроксида кальция с азотной кислотой в молекулярном и ионном виде.
Сохраните или поделитесь с одноклассниками: